| 物竞编号 | 05N2 |
|---|---|
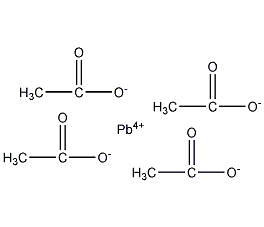
| 分子式 | C8H12O8Pb |
| 分子量 | 443.38 |
| 标签 | 醋酸高铅, 四乙酸铅, 乙酸高铅盐, 四醋酸铅, 乙酸高铅, 乙酸铅(Ⅳ), lead tetraacetate, LTA, 氧化剂 |
编号系统
CAS号:546-67-8
MDL号:MFCD00008693
EINECS号:208-908-0
RTECS号:AI5300000
BRN号:3595640
PubChem号:暂无
物性数据
1. 性状:白色棱状吸湿性晶体
2. 密度(g/ cm3,25/4℃):2.228
3. 相对蒸汽密度(g/cm3,空气=1):未确定
4. 熔点(ºC):175-180
5. 沸点(ºC,常压):118.1
6. 沸点(ºC,8kPa):未确定
7. 折射率:未确定
8. 闪点(ºC):未确定
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC):未确定
11. 蒸气压(kPa,25ºC):未确定
12. 饱和蒸气压(kPa,55.1ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:四乙酸铅在热的冰乙酸中溶解度很大,在冷溶液中溶解度较小(室温时约为0.072 mol/L), 可以溶解于苯、二氯甲烷、三氯甲烷、四氯化碳、三氯乙烷、硝基苯、乙腈等有机溶剂,但是溶解度不大。遇水立刻分解为棕黑色的二氧化铅和乙酸。
毒理学数据
暂无
生态学数据
该物质对环境可能有危害,对水体应给予特别注意。
分子结构数据
暂无
计算化学数据
1、 疏水参数计算参考值(XlogP):
2、 氢键供体数量:0
3、 氢键受体数量:8
4、 可旋转化学键数量:0
5、 互变异构体数量:
6、 拓扑分子极性表面积(TPSA):161
7、 重原子数量:17
8、 表面电荷:-4
9、 复杂度:25.5
10、 同位素原子数量:0
11、 确定原子立构中心数量:0
12、 不确定原子立构中心数量:0
13、 确定化学键立构中心数量:0
14、 不确定化学键立构中心数量:0
15、 共价键单元数量:5
性质与稳定性
1.按规格使用和贮存,不会发生分解,避免与氧化物接触。溶于热的冰醋酸,可用醋酸作重结晶溶剂。溶于无水苯、无水氯仿、四氯化碳等溶剂中。溶于浓氢卤酸中,生成H2PbX6。在空气中不稳定,易吸潮水解。遇湿气或水水解生成棕色的二氧化铅沉淀。使其活性有所降低。如呈黑色,临用前应重结晶。若将醋酸铅(Ⅳ)避光储存在放有固体氢氧化钾及五氧化二磷作干燥剂的真空保干器中,可以保存数周。有毒,为致癌物。应避免与皮肤接触,在有机合成中用作选择性氧化剂及芳香化合物的铅烷化反应。
2.具有强烈的氧化性能,本身虽不燃烧,但在一定的条件下,经受摩擦、震动、撞击、高热或遇酸碱的物质,在受潮,接触有机物、还原剂以及和性质有抵触的物品混存时,即能分解,发生燃烧和爆炸。四乙酸铅有剧毒,不要和皮肤接触。
贮存方法
储存于阴凉、干燥、通风良好的库房。远离火种、热源。防止阳光直射。包装密封。应与酸类、食用化学品分开存放,切忌混储。储区应备有合适的材料收容泄漏物。
合成方法
制法:在2 L圆底烧瓶中放置1080 g冰醋酸和360 g乙酸酐,600 g Pb3O4在搅拌下分小量加入,维持温度不超过65 oC,加完后升温到65 oC继续搅拌直到固体完全溶解。冷却到室温,过滤,用冰醋酸洗涤得到固体约300 g,在真空干燥器中干燥 (式1)[1]。母液回到原反应瓶中,加热到 80 oC,搅拌下通入干燥的氯气,反应完毕后趁热过滤掉氯化铅,并用冰醋酸洗涤。滤液冷却过滤,固体用冰醋酸重结晶,又可以得到一部分四乙酸铅 (式2)。
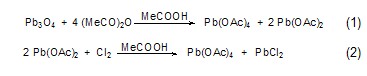
用途
1. 在乙酸溶液中用作氧化剂。氧化二酚成醌,硫醇成二硫化物,酰胺成异氰酸酯,连二醇成二分子醛酮,苯乙烯成苯乙醛。羟酸卤化脱羧。烯烃、肟、腙的乙酰氧基化,环丙烷的分裂等等。
2.四乙酸铅在有机合成中用作氧化剂,它能氧化不饱和烃和芳香烃,氧化单羟基醇为环醚;实现1,2-二醇的断裂;酮的乙酰化;羧酸的脱羧;氧化转移含氮基团等。
一元酚可以被Pb(OAc)4氧化成醌,但是产率不高。对位或者邻位二酚可以被Pb(OAc)4氧化成醌 (式3,式4)[2],这一反应是快速而定量的。

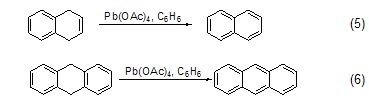
Pb(OAc)4也可以使部分氢化的芳环或者杂环芳化 (式5,式6)[3],但是不如溴、氯醌等用得普遍。
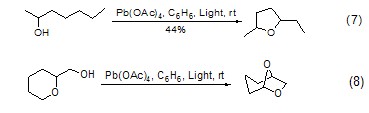
Pb(OAc)4在吡啶中将伯醇和仲醇氧化成醛和酮[4]。如果将二元醇和四乙酸铅的苯溶液常温下用紫外线照射,可以环化得到内醚,一般多是四氢呋喃的衍生物 (式7,式8)[5,6],有些反应可以作为制备方法。
Pb(OAc)4对邻二醇的氧化反应是它的一个重要方面,Pb(OAc)4只对1,2-二醇起反应 (式9,式10)[7],对于1,3-二醇、1,4-二醇就不容易起反应。

近年发现对于不饱和的1,2-二醇,氧化产物立刻进行分子内环加成反应得到有用的环化物 (式11,式12)[8,9]。

一元羧酸在醋酸铜的催化作用下可以被氧化脱羧形成烯烃 (式13)[10],产率相当好。

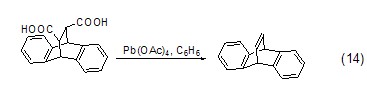
而邻二羧酸可以直接被四乙酸铅氧化脱去两个羧基,形成烯烃 (式14)[11]。邻二羧酸的脱羧反应可以用来合成一些特殊的烯烃。
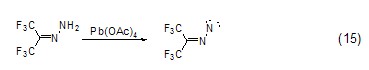
一些伯胺可以被Pb(OAc)4氧化成氮烯[12], 简单的腙则被氧化成重氮化合物 (式15)[13]。
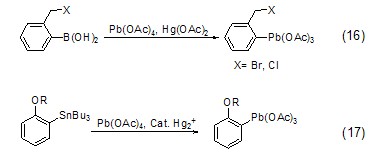
此外一些有机硼、有机锡化合物可以被四乙酸铅转化为四价的有机铅化合物 (式16,式17)[14,15]。
安全信息
危险运输编码:UN 1616 6.1/PG 3
危险品标志: 有毒
有毒  危害环境
危害环境
文献
1. Bailar, J. C. Jr. Inorg. Syn., 1939, 1, 47. 2. Dimroth, O.; Friedmann, O.; Kammerer, H. Ber., 1920, 53, 481. 3. Ciegee, R. Ann., 1930, 481, 263. 4. Ciegee, R. Ann., 1930, 481, 263. 5. Partch, R. E. Tetrahedron Lett., 1964, 3071. 6. Mihailović, M. Lj.; Čeković, Ž.; Maksimović,Z.; Jeremić, D.; Lorenc, Lj.; Mamuzić, R. I. Tetrahedron, 1965, 21, 2799. 7. Wolf, F. J.; Weijlard, J. Org. Syn. Coll., 1939, 4, 124. 8. Fernandez, E. M. S.; Lena J. I. C.; Altinel, E.; Birlirakis, N.; Barrerob, A. F.; Arseniyadis, S. Tetrahedron: Asymmetry, 2003, 2277. 9. Unaleroglu, C.; Aviyente, V.; Arseniyadis, S. J. Org. Chem., 2002, 67, 2447. 10. Bacha, J. O.; Kochi., J. K. Tetrahedron, 1968, 24, 2215. 11. Tamelen, E. E.; Pappas, S. P. J. Am. Chem. Soc., 1963, 85, 3297. 12. Nagata, W., Syn. Commun., 1972, 2, 11. 13. Middleton, W. J.; Gale D. M. Org. Syn., 1970, 50, 6. 14. Fedorov A. Y.; Carraraa, F.; Fineta, J.-P. Tetrahedron Lett., 2001, 42, 5875. 15. Fedorov, A. Y.; Fineta, J. -P. Eur. J. Org. Chem., 2004, 2040. 16.参考书:现代有机合成试剂<性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号