| 物竞编号 | 02BA |
|---|---|
| 分子式 | C3H3NS2 |
| 分子量 | 119.21 |
| 标签 | 2-巯基-2-噻唑啉, 2-Thiazoline-2-thiol, 1,3-Thiazolidine-2-thione |
编号系统
CAS号:96-53-7
MDL号:MFCD00126013
EINECS号:202-512-1
RTECS号:XJ6122000
BRN号:106332
PubChem号:24897083
物性数据
1. 性状:浅棕色货白色固体,有恶臭。
2. 密度(g/mL,20℃):未确定
3. 相对蒸汽密度(g/mL,空气=1):未确定
4. 熔点(ºC): 105-107
5. 沸点(ºC,常压):未确定
6. 沸点(ºC, kPa):未确定
7. 折射率:未确定
8. 闪点(ºC):未确定
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC): 未确定
11. 蒸气压(mmHg,ºC):未确定
12. 饱和蒸气压(kPa, ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:溶于CH2Cl2和大多数极性有机溶剂。通常在CH2Cl2中使用。
毒理学数据
1. 急性毒性:
大鼠经口LD50:300mg/kg;
大鼠腹膜腔LDL0:500mg/kg;
小鼠经口LDL0:710mg /kg;
小鼠腹膜腔LD50:200mg/kg;
生态学数据
该物质对水有稍微的危害。
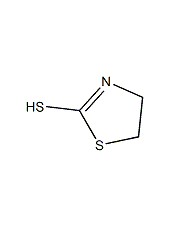
分子结构数据
1、 摩尔折射率:30.90
2、 摩尔体积(cm3/mol):84.7
3、 等张比容(90.2K):233.0
4、 表面张力(dyne/cm):57.2
5、 极化率(10-24cm3):12.25
计算化学数据
1.疏水参数计算参考值(XlogP):0.9
2.氢键供体数量:1
3.氢键受体数量:2
4.可旋转化学键数量:0
5.互变异构体数量:2
6.拓扑分子极性表面积69.4
7.重原子数量:6
8.表面电荷:0
9.复杂度:71.2
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.避免与氧化物接触。
2.对空气和湿气稳定。由于其衍生物显示出多种生物活性,建议在通风橱中操作和使用。
贮存方法
合成方法
通过氨基乙基硫酸酯与二硫化碳在碱催化下制备[1]。
用途
1. 用作酸性光亮镀铜添加剂,医药中间体。
2. 1,3-噻唑烷-2-硫酮在有机合成中的作用主要是通过它与羧酸或者酰卤反应生成的酰胺衍生物来表现。当1,3-噻唑烷-2-硫酮生成酰胺衍生物之后,酰基的反应活性得到活化。例如:酰胺可以被DIBAL-H选择性还原生成相应的醛,或者在其它酯基或者酰胺的存在下被NaBH4还原生成相应的醇[2]。但是这些功能已经被其它反应试剂和条件所覆盖。目前,1,3-噻唑烷-2-硫酮酰胺衍生物主要被用于氨基和羟基的选择性酰化试剂。
1,3-噻唑烷-2-硫酮与羧酸在缩合试剂DCC的存在下生成酰胺,也可以与酰卤在三乙胺和DMAP存在下生成酰胺。生成的酰胺衍生物与氨基化合物在中性条件下室温放置或者共热可使1,3-噻唑烷-2-硫酮离去而生成新的酰胺。该反应还常常用于大环化合物的反应,一般给出非常满意的产率[3]。如果有不同官能团存在时,也表现出高度的化学选择性 (式1~式3)[4,5]。
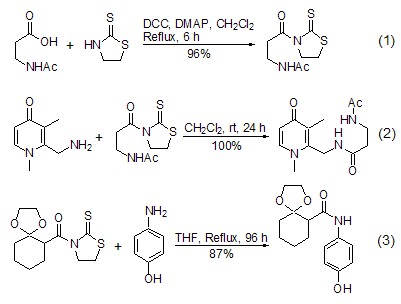
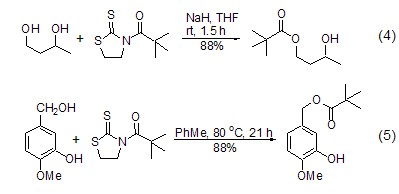
1,3-噻唑烷-2-硫酮酰胺衍生物与醇一起共热可以方便地得到相应的酯[6~8]。当有不同的醇同时存在时,使用该方法可达到高度的区域选择性。选择性一方面决定于酰胺衍生物中酰基片段位阻的大小,叔戊酰基给出最好的结果。另一方面决定于羟基的类型,活性次序是伯醇>仲醇>酚 (式4,式5)[7,8]。
安全信息
危险运输编码:UN 2811 6.1/PG 3
危险品标志: 有害
有害
安全标识:S24/25
危险标识:R22
文献
1. Dewey, C. S.; Bafford, R. A. J. Org. Chem., 1965, 30, 491. 2. Nagao, Y.; Kawabata, K.; Seno, K.; Fujita, E. J. Chem. Soc., 1980, 2470. 3. Wei, W.; Tomohiro, T.; Kodaka, M.; Okuno, H. J. Org. Chem., 2000, 65, 8979. 4. Liu, Z. D.; Kayyali, R.; Hider, R. C.; Poter, J. B.; Theobald, A. E. J. Med. Chem., 2002, 45, 631. 5. Nicolaou, K. C.; Dai, W.-M. J. Am. Chem. Soc., 1992, 114, 8908. 6. Brown, G. R.; Clarke, D. S.; Faull, A. W.; Foubister, A. J.; Smithers, M. J. Bioorg. Med. Chem. Lett., 1996, 6, 273. 7. Yamada, S. J. Org. Chem., 1992, 57, 1591. 8. Yamada, S.; Sugaki, T.; Matsuzaki, K. J. Org. Chem., 1996, 61, 5932. 9.参考书:现代有机合成试剂<性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无



 沪公网安备 31010602001115号
沪公网安备 31010602001115号