| 物竞编号 | 0JX4 |
|---|---|
| 分子式 | HCl |
| 分子量 | 36.46 |
| 标签 | 氯化氢, 酸性溶剂, 氯化物沉淀剂, 氯离子配合剂, pH调节剂, 激光材料 |
编号系统
CAS号:7647-01-0
MDL号:MFCD00011324
EINECS号:231-595-7
RTECS号:MW4025000
BRN号:1098214
PubChem号:24845468
物性数据
1.性状:无色有刺激性气味的气体。[1]
2.熔点(℃):-114.2[2]
3.沸点(℃):-85.0[3]
4.相对密度(水=1):1.19[4]
5.相对蒸气密度(空气=1):1.27[5]
6.饱和蒸气压(kPa):4225.6(20℃)[6]
7.临界温度(℃):51.4[7]
8.临界压力(MPa):8.26[8]
9.辛醇/水分配系数:0.25[9]
10.溶解性:易溶于水,溶于乙醇、乙醚。[10]
毒理学数据
1、
试验方法:吸入
摄入剂量:450 mg/m3/1H ,女性一天(县)前交配
测试对象:啮齿动物-鼠
毒性类型:生殖
毒性作用:1.对胚胎或胎儿有影响(除死亡,如发育迟缓胎儿)
2.具体的发展异常-稳态
2、
试验方法:吸入
摄入剂量:1108年ppm/1H
测试对象:啮齿动物-鼠
毒性类型:急性
毒性作用:1.特别感官(眼)异常
2.肺,胸部或呼吸-呼吸刺激
3、
试验方法:腹腔
摄入剂量:40142微克/千克
测试对象:啮齿动物-鼠
毒性类型:急性
毒性作用:详细的毒副作用没有报告以外的其他致死剂量值。
4.急性毒性[11]
LD50:900mg/kg(大鼠经口)
LC50:4600mg/m3,3124ppm(大鼠吸入,1h)
5.刺激性[12] 家兔经眼:5mg(30s),轻度刺激。
6.其他[13] LCLo:1300ppm(人吸入30min);3000ppm(人吸入5min)
生态学数据
该物质对环境可能有危害,对水体应给予特别注意。
分子结构数据
1、摩尔折射率:无可用
2、摩尔体积(cm3/mol):无可用
3、等张比容(90.2K):无可用
4、表面张力(dyne/cm):无可用
5、极化率:无可用
计算化学数据
1、疏水参数计算参考值(XlogP):0.8
2、氢键供体数量:1
3、氢键受体数量:0
4、可旋转化学键数量:0
5、互变异构体数量:无
6、拓扑分子极性表面积(TPSA):0
7、重原子数量:1
8、表面电荷:0
9、复杂度:0
10、同位素原子数量:0
11、确定原子立构中心数量:0
12、不确定原子立构中心数量:0
13、确定化学键立构中心数量:0
14、不确定化学键立构中心数量:0
15、共价键单元数量:1
性质与稳定性
1.易溶于水,有强烈的腐蚀性,能腐蚀金属,对动植物纤维和人体肌肤均有腐蚀作用。浓盐酸在空气中发烟,触及氨蒸气会生成白色云雾。氯化氢气体对动植物有害。盐酸是极强的无机酸,与金属作用能生成金属氯化物并放出氢;与金属氧化物作用生成盐和水;与碱起中和反应生成盐和水;与盐类能起复分解反应生成新的盐和新的酸。与各种有机物容易进行反应。剧毒!
2.当15℃时1体积水溶解约450体积HCl。17℃时1体积乙醇可溶327体积的HCl。
3.稳定性[14] 稳定
4.禁配物[15] 碱类、活性金属粉末
5.聚合危害[16] 不聚合
贮存方法
储存注意事项[17] 储存于阴凉、通风的不燃气体专用库房。远离火种、热源。库温不宜超过30℃。应与碱类、活性金属粉末分开存放,切忌混储。储区应备有泄漏应急处理设备。
合成方法
1.精馏法以工业盐酸为原料,经精馏,冷凝分离除去杂质后,再经超净过滤除去杂质,制得无色透明的BV-1级盐酸。

图XVII-6用盐酸生产氯化氢的装置
2.盐酸生产方法主要是合成法。
在电解食盐水生产烧碱的同时,可得到氯气和氢气,经过水分离后的氯气和氢气,通人合成炉进行燃烧生成氯化氢气体.经冷却后用水吸收制得盐酸成品。尾气经吸收后排空。其反应方程式如下:
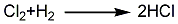
3.氯化氢精馏提纯法以98%~99%的工业氯化氢为原料,经冷冻除水后,再经常温吸附器、低温吸附器及中压吸附器吸附,进入精馏塔精馏,再经低温吸附,冷凝后,制得99.995%高纯氯化氢成品。
直接合成精馏提纯法由氢和氯直接合成氯化氢后,再经吸附、精馏、提纯,制得高纯氯化氢成品。
4.将经过水分离的氢气和氯气通入合成炉,燃烧生成氯化氢气体,冷却后用水吸收,而尾气经吸收后由水流泵排空。反应方程式如下:
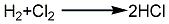
5.盐酸法将由盐酸合成塔制造的35%盐酸送人无水氯化氢发生装置,发生氯化氢气体,经冷却脱湿,进一步导人干燥塔进行脱湿干燥精制后,通过压缩机压缩,经液化器冷却液化后,放入贮槽贮存,再压人钢制高压气体容器中。
6.使纯的浓盐酸流入浓硫酸中,氯化氢的装置斗上安装一个容量约为200mL的滴液漏斗,以约40cm长的毛细管作为滴液管。分液漏斗中装200mL浓硫酸,毛细管部分事先也装满盐酸。毛细管插到浓H2SO4液面之下。盐酸通过毛细管一点一点流下,就可以得到均匀的氯化氢气流。调节滴液漏斗旋塞,就可以按所需的产气速度滴加盐酸。滴完200mL浓盐酸后使产气停止,更换新的硫酸。每200mL浓盐酸可发生67.4g HCl。
使生成的气体通过一个盛有浓H2SO4的洗瓶以除去其中可能存在的湿气,然后在用液态空气冷凝的冷凝器中凝结。经分馏并取中间馏分可得高纯度的HCl气体。即可得HCl气。设备如图。在容量为500~1000mL的分液漏图用盐酸生产。(1)化氢精馏提纯法 以98%~99%的工业氯化氢为原料,经冷冻除水后,再经常温吸附器、低温吸附器及中压吸附器吸附,进入精馏塔精馏,再经低温吸附,冷凝后,制得99.995%高纯氯化氢成品。(2)直接合成精馏提纯法 由氢和氯直接合成氯化氢后,再经吸附、精馏、提纯,制得高纯氯化氢产品。
采用精馏法。以工业盐酸为原料,经精馏、冷凝分离除去杂质后,再经超净过滤除去杂质,制得无色透明的BV-1级盐酸。
7.在200g工业盐酸 (29% ~31%)中加入1kg的10%二氯化锡的盐酸溶液,搅拌,进行脱色。脱色完全后,在搅拌下加入0.07g的氯化钡,混合均匀后,静置6h以上,使沉淀完全,以除去 SO42- 离子等杂质。然后进行减压蒸馏,蒸馏速度不宜过快,先逸出的氯化氢气体用20%的盐酸吸收,使盐酸含量提高到36%~38% (相对密度为1.185~1.195),即为成品。当108.5℃时 蒸 出 恒 沸 物,冷 凝 后 为20.4%的盐酸,接入稀酸瓶,留作吸收氯化氢气体用。
用途
1.基本化工原料,用于石油、化工、冶金、印染、食品等工业部门。
2.用于制造医药品的原料、染料中间体、无机盐化合物、增塑剂原料的制造。用于制造氯乙烯等合成树脂,制造氯乙烷、氯代甲烷、半导体的精制。用于制盐酸。
3.用于制造各种氯化物、染料及医药中间体、氯丁橡胶等,还用于湿法冶金,金属表面处理、制糖和制革工艺等。
4.用作分析试剂及腐蚀剂,也用于氯化物制取。
5.用于制盐酸、氯化物,并用作有机化学的缩合剂等。
6.主要用于食品、医药、精细化学品生产,也可用于化学试剂。
7.作pH调节剂,可用于水解淀粉制糖浆,也可用于橘子罐头生产中的去络和脱囊,按生产需要适量使用。
8.用于半导体制备工艺中的外延、热氧化、扩散、蚀刻、化学气相淀积(CVD)等工序,还可用于发光二极管、激光器和光导纤维的生产。是电子工业大规模集成电路所需的重要材料之一。
9.是制造氯化铵、氯化钙、氯化锌、氯化亚铜、碱式氯化铝、三氯化铁液体等氯化物的原料。在染料及医药中间体的合成中.用于氨基重氮化、硝基转化为氨基、磺酸钠盐转化为磺酸等。也用于聚氯己烯、氯丁橡胶、氯乙烷的合成。还用于湿法冶金(如分解钨矿石生产钨酸等),金属表面处理(作为铜材酸洗除锈)。在印染工业中,用于织物漂白后酸洗、丝光处理后中和等。此外,也用于离子交换树脂的再生、制糖和制革工业。
10.用作酸性清洗腐蚀剂,可与双氧水配合使用。以盐酸为主剂进行化学清洗具有作用力强、速度快、效果明显、使用方便、所需费用低等优点,适用于碳素钢、铜,但不能用于奥氏体不锈钢、钛等材质的化学清洗。
11.主要用于电子工业,在集成电路生产中用于蚀刻、钝化、外延等工艺。还用于金属冶炼和光导通讯领域。
12.用于制染料、香料、药物、各种氯化物及腐蚀抑制剂。[18]
安全信息
危险运输编码:暂无
危险品标志: 腐蚀
腐蚀
安全标识:S26 S45 S36/S37/S39
文献
[1~18]参考书:危险化学品安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8
备注
2647-01-0





 沪公网安备 31010602001115号
沪公网安备 31010602001115号