| 物竞编号 | 0QCL |
|---|---|
| 分子式 | C10H18O5 |
| 分子量 | 218.25 |
| 标签 | (Boc)2O, 肽合成用 |
编号系统
CAS号:24424-99-5
MDL号:MFCD00008805
EINECS号:246-240-1
RTECS号:HT0230000
BRN号:1911173
PubChem号:24862282
物性数据
1. 性状:白色低熔点固体
2. 密度(g/mL,25/4℃):0.949
3. 相对蒸汽密度(g/mL,空气=1):未确定
4. 熔点(ºC):22-24
5. 沸点(ºC,0.5torr):56-57
6. 沸点(ºC,5.2kPa):未确定
7. 折射率:1.4075-1.4095
8. 闪点(ºC):37
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC):未确定
11. 蒸气压(kpa,20ºC):未确定
12. 饱和蒸气压(kPa,60ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:溶于大多数有机溶剂,如四氯化碳、四氢呋喃、二氧杂环己烷、醇、丙酮、乙腈、N,N-二甲基甲酰胺等,不溶于冷水。
毒理学数据
在皮肤上:造成腐蚀性影响。刺激皮肤和粘膜。
在眼睛上:强烈的腐蚀性影响。刺激的作用。
致敏作用:通过皮肤接触可能造成敏化作用。
生态学数据
对水是稍微危害的,若无政府许可,勿将材料排入周围环境。
分子结构数据
1、 摩尔折射率:53.60
2、 摩尔体积(cm3/mol):207.0
3、 等张比容(90.2K):489.3
4、 表面张力(dyne/cm):31.2
5、 极化率(10-24cm3):21.25
计算化学数据
1.疏水参数计算参考值(XlogP):2.7
2.氢键供体数量:0
3.氢键受体数量:5
4.可旋转化学键数量:6
5.互变异构体数量:无
6.拓扑分子极性表面积61.8
7.重原子数量:15
8.表面电荷:0
9.复杂度:218
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.如果遵照规格使用和储存则不会分解
避免接触氧化物,水分/潮湿,热
2.对湿气敏感,易燃,需保存在冰箱中,使用温度不可超过80 oC。
贮存方法
1.2-8℃干性的保护气体下处置。
2.保持贮藏器密封,放入紧密的贮藏器内,储存在阴凉,干燥的地方。
合成方法
1.叔丁醇钾溶于无水四氢呋喃,在-5~-20℃通入干燥的二氧化碳,生成浆状物,继续保持低温,滴加光气苯溶液,制得三碳酸二叔丁酯。将其溶于四氯化碳,加适量1,4-二氮杂二环[2,2,2]辛烷,在25℃搅拌使二氧化碳释放完全,转化为二碳酸二叔丁酯。
2.注意!使用剧毒性的光气,应在通风厨内小心操作。凡粘有光气溶掖的玻璃器皿,均应清洗后方可拿出通风橱。
(1)制三碳酸二叔丁酯
将装有机械搅拌器,200毫升恒压滴压漏斗,氯化钙干燥管,伸近瓶底的内径不小于6毫米的1升三颈烧瓶烘干。事先校准并标出滴液漏斗盛装85毫升和105毫升液体的水平面。通入干燥氮气,烧瓶中加入44.8克(0.40摩尔)不含醇的叔丁醇钾和550毫升无水四氢吠喃,搅拌5-10分钟使成溶液。将反应瓶浸入冰盐浴以保持-5一-20℃,在剧烈搅拌下,通入干燥二氧化碳,大约30分钟,生成稠密的浆状物。与此同时,将86毫升无水苯加入滴液漏斗中,并鼓入光气泡,直到光气在苯中的溶液体积达105毫升为止,相当于含有24克(0.24摩尔)的光气。当二氧化碳的加成反应完成后,在剧烈搅拌下将光气溶液滴加到冷却的反应物中,约需1小时,冷浴温度保持在-5~-10℃,反应混合物粘度变小,仍为白色乳状物。当光气的加成反应完成后,继续搅拌,45分钟,同时通入无水氮乙毛以吹出大部分的过量光气。卸除烧瓶上的仪器,塞上二颈,在减压下用旋转蒸发器将约650毫升溶剂浓缩至100毫升,烧瓶仍用冰盐浴冷却以保持一5一0℃。由于反应混合物中残余少量光气,应将抽气泵或真空泵废气排入通风橱,收集在冷阱中的物料也在通风橱内抽空,含有很细分散的氯化钾的残余物用大口径砂芯漏斗吸滤,漏斗在用前经50毫升冰冷的戊烷进行预冷。过滤时,用一个大口径漏斗将过滤漏斗反盖着,并通入氮气使物料隔除潮湿空气,用J}}毫升冰冷的戊烷将烧瓶中残余物洗入过滤漏斗中,然后用2*100毫升冰冷的戊烷洗涤滤渣。滤液与戊烷洗涤液合并,在0℃减压下,用旋转蒸发器浓缩至于,得白色固体,重33.7克,将粗品溶于1250毫升戊烷,冷至-15℃ ,拆出白色晶体。母液经旋转蒸发器浓缩后还可得到两批晶体,总计得到三碳酸二叔丁酯纯品31.2-32.8(59~62%),为白色晶体,熔点 62~63℃(分解)。
(2)制二碳酸二叔丁酚
在放有电磁搅拌棒的烧杯中,加入20.0克(0 .076摩尔)三碳酸二叔丁醋溶于了i}毫升四氯化碳的溶液和0.10克(0.0009摩尔)新升华的1.4一二氮杂二环〔2·2·2〕辛烷,立即迅速地释放出二氧化碳。在25℃搅拌45分钟使二氧化碳释放完全,然后加入足以使水层为弱酸性的含有适量柠檬酸的35毫升水溶液。分出有机层,用无水硫酸镁干燥,在25℃用旋转蒸发器浓缩,残余液经减压蒸馏,得到二碳酸二叔丁酚无色液体产13.3---15.1克(80~91%)用三乙胺作催化剂也得到类似结果。但三乙胺不如1,4-二氮杂二环辛烷有效,因为三乙胺与溶剂可能反应,且与产物的分离较困难。
3.在1,4-二氮杂二环[2.2.2]辛烷的催化下,将碳酰氯与碳酸叔丁酯直接反应而制备。
用途
1.用作医药及有机合成中间体,是一种重要的应用于医药及农化产品合成的氨基保护剂。
2.在有机化学反应中,(Boc)2O常作为胺、酚、硫醇、酰胺、内酰胺、氨基甲酸酯等底物的叔丁氧羰基化试剂,该反应速率很快,产率也比较高。
叔丁氧羰基化反应(官能团的保护) 由于酰卤试剂的稳定性较差,因此 (Boc)2O被广泛用作氨基的保护基团[1,2],该保护基团在三氟乙酸的作用下可脱去。脂肪胺、脂环胺、芳香胺以及杂环胺类均能够与(Boc)2O反应。在适当的条件下,多官能团化合物如二胺 (式1)、氨基醇、氨基酸等也能够选择性地与(Boc)2O反应[3]。

在适当的条件下,酚、醇、烯醇以及硫醇也能与 (Boc)2O在羟基等官能团上反应而进行Boc保护。
而对其它含氮化合物,如酰胺、内酰胺、氨基甲酸酯等,(Boc)2O同样可以作为一种比较好的保护试剂,它在无水条件下,能够与亲核性很弱的酰胺和氨基甲酸酯发生反应;在三乙胺和N,N-二甲基氨基吡啶(DMAP)存在下,以CH2Cl2为溶剂,二级酰胺和内酰胺化合物也可以采用Boc保护 (式2)[4,5]。
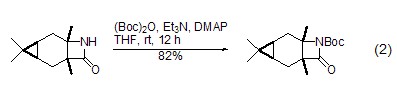
此外,碳负离子、席夫碱均能够在适当条件下与 (Boc)2O反应,生成相应的叔丁氧羰基化合物 (式3)[6]。
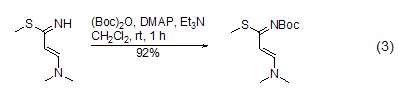
氨基保护基的交换 苄氧羰基(Cbz)、Fmoc等也常作为氨基的保护基团,在稍过量的 (Boc)2O存在时,被Cbz、Fmoc保护的氨基化合物可发生保护基交换,转化为Boc保护的氨基化合物 (式4)[7]。
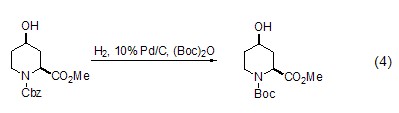
羧基的活化 (Boc)2O除了可作为保护基外,还可作为羧基的活化基团 (式5),这主要是因为Boc基团是一种比较好的离去基团,与羧基反应之后,在适当的条件下可以离去,从而使羧基部分处于非电中性状态而带有较好的亲电性[8]。
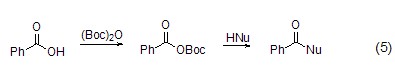
安全信息
危险运输编码:暂无
危险品标志:暂无
安全标识:暂无
危险标识:暂无
文献
1. Liu, G.; Sieburth, S. M. Org. Lett., 2003, 5, 4677. 2. Ouchi, T.; Uchida, T.; Arimura, H.; Ohya, Y. Biomacromolecules, 2003, 4, 477. 3. Busnel, O.; Carreaux, F.; Carboni, B.; Pethe, S.; Goff, S. V.-L.; Mansuy, D.; Boucher, J.-L. Bioorg. Med. Chem., 2005, 13, 2373. 4. Gyonfalvi, S.; Szakonyi, Z.; Fulop, F. Tetrahedron: Asymmetry, 2003, 14, 3965. 5. Janetka, J. W.; Furness, M. S.; Zhang, X.; Coop, A.; Folk, J. E.; Mattson, M. V.; Jacobson, A. E.; Rice, K. C. J. Org. Chem., 2003, 68, 3976. 6. Robin, A.; Julienne, K.; Meslin, J. C.; Deniaud, D. Tetrahedron Lett., 2004, 45, 9557. 7. Lloyd, R. C.; Smith, M. E. B.; Brick, D.; Taylor, S. J. C.; Chaplin, D. A.; McCague, R. Org. Process Res. Dev., 2002, 6, 762. 8. Ma, D. W.; Xia, C. F. Org. Lett., 2001, 3, 2583. 9.参考书:现代有机合成试剂<性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号