| 物竞编号 | 0S4X |
|---|---|
| 分子式 | C10H16O4S |
| 分子量 | 232.30 |
| 标签 | 7,7-三甲基二环[2.2.1]庚烷-2-酮-1-甲磺酸, 左旋樟脑磺酸, L-(-)樟脑磺酸, (1R)-(-)-樟脑磺酸, 手性试剂, 酸催化剂 |
编号系统
CAS号:35963-20-3
MDL号:MFCD00150753
EINECS号:252-817-9
RTECS号:暂无
BRN号:2809676
PubChem号:暂无
物性数据
1. 性状:白色晶体
2. 密度(g/mL,20℃):未确定
3. 相对蒸汽密度(g/mL,空气=1): 未确定
4. 熔点(ºC):197-199
5. 沸点(ºC,常压): 未确定
6. 沸点(ºC,35mm hg):未确定
7. 折射率:-21.5 ° (C=5, H2O)
8. 闪点(ºC):未确定
9. 比旋光度(º):-22 º (c=20,H2O)
10. 自燃点或引燃温度(ºC): 未确定
11. 蒸气压(kPa,25ºC):未确定
12. 饱和蒸气压(kPa,60ºC): 未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:溶于水
毒理学数据
主要的刺激性影响:
在皮肤上面:在皮肤和黏膜上造成腐蚀性影响
刺激皮肤和黏膜。
在眼睛上面:强烈的腐蚀性影响
刺激的影响。
致敏作用:没有已知的敏化影响。
生态学数据
对水是稍微有危害的不要让未稀释或大量的产品接触地下水、水道或者污水系统,若无政府许可,勿将材料排入周围环境。
分子结构数据
暂无
计算化学数据
1、 疏水参数计算参考值(XlogP):0.5
2、 氢键供体数量:1
3、 氢键受体数量:4
4、 可旋转化学键数量:2
5、 拓扑分子极性表面积(TPSA):74.1
6、 重原子数量:15
7、 表面电荷:0
8、 复杂度:404
9、 同位素原子数量:0
10、 确定原子立构中心数量:1
11、 不确定原子立构中心数量:1
12、 确定化学键立构中心数量:0
13、 不确定化学键立构中心数量:0
14、 共价键单元数量:1
性质与稳定性
1.常规情况下不会分解,没有危险反应。
2.容易吸湿,有腐蚀性。
贮存方法
密封、阴凉、干燥、通风保存
合成方法
暂无
用途
CSA可用作酸催化剂和手性辅助试剂等。
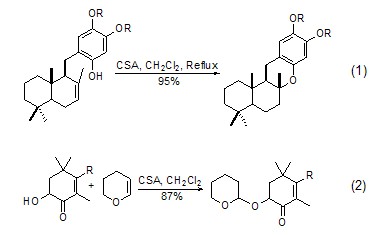
作为酸催化剂 CSA广泛地用作有机合成中的酸催化剂,经常用于催化羟基与烯烃、醛、酮的加成生成醚或缩醛、缩酮。反应通常在二氯甲烷溶剂中进行,并具有良好的立体选择性,这是来源于CSA本身的独特结构。如CSA催化分子内羟基对烯键的立体选择性加成关环 (式1)[1]。这类反应也常用于保护羟基,如使用二氢吡喃和催化量的CSA可以生成含有四氢吡喃基的醚 (式2)[2]。
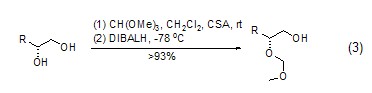
在CSA催化下,1,2-二醇、1,3-二醇与原甲酸三甲酯反应生成具有立体选择性的环状原甲酸酯,然后它被二异丁基氢化锂铝 (DIBALH) 还原为醇醚 (式3)[3]。
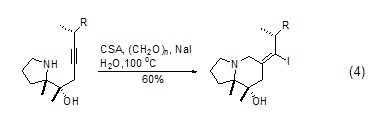
CSA也可用在由亲核试剂促进的炔-亚氨基环化反应中,如烷基胺与甲醛和碘化钠反应生成高产率哌啶衍生物 (式4)[4]。
对于环氧化物的分子内开环反应,CSA是最有效的催化剂。含氧杂环的大小高度地依赖于羟基环氧化物的结构。当在环氧化物的另一侧α位上有饱和碳链时,生成四氢呋喃衍生物 (式5)[5]。而当此位置上有富电子的双键时,因双键稳定了亲核取代的中间体,反应采取不同机理而生成四氢吡喃的衍生物 (式6)[6]。此方法也可推广到八元环的合成 (式7)[7]。

CSA也可用于催化螺缩醛的合成,在分子内羟基位置合适时有良好的产率和立体选择性 (式8)[8]。

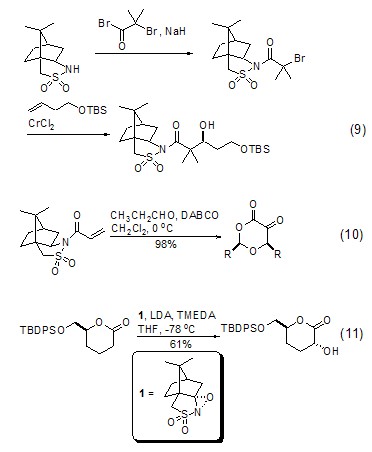
手性辅助剂 CSA具有独特的空间结构,因而它的衍生化通常具有良好的立体选择性,且反应后,樟脑环又可方便地脱去 (式9,式10)[9,10]。这些衍生化反应包括取代、缩合、加成等。
氧氮杂环 樟脑衍生的氧氮杂环丙烷可用在硫化物和二硫化物的非对称氧化反应中,生成亚砜和硫代亚磺酸酯;也可用在烯烃的环氧化反应中。对于酯、酰胺和酮的烯醇锂的羟基化反应,樟脑衍生的氧氮杂环丙烷是首选试剂 (式11)[11]。
安全信息
危险运输编码:UN 3261 8/PG 2
危险品标志: 腐蚀
腐蚀
安全标识:暂无
危险标识:暂无
文献
1. Alvarez-Manzaneda, E. J.; Chahboun, R.; Barranco, P. I.; Cabrera E.; Alvarez, E.; Alvarez-Manzaneda, R. Org. Lett., 2005, 7, 1477. 2. Choi, S.; Koo, S. J. Org. Chem., 2005, 70, 3328. 3. He, L. L.; Byun, H. S.; Bittman, R. J. Org. Chem., 2000, 65, 7618. 4. Lin, N. H.; Overman, L. E.; Rabinowitz, M. H.; Robinson, L. A.; Sharp, M. J.; Zablocki, J. J. Am. Chem. Soc., 1996, 118, 9062. 5. Morimoto, Y.; Nishikawa, Y.; Takaishi, M. J. Am. Chem. Soc., 2005, 127, 5806. 6. Kadota, I.; Yamamoto, Y. J. Org. Chem., 1998, 63, 6597. 7. Matsukura, H.; Morimoto, M.; Koshino, H.; Nakata, T. Tetrohedron Lett., 1997, 38, 5545. 8. Patra, D.; Yang, L. H.; Totah, N. I. Tetrahedron, 2000, 56, 507. 9. Storer, R. I.; Takemoto, T.; Jackson, P. S.; Brown, D. S.; Baxendale, I. R.; Ley, S. V. Chem. Eur. J., 2004, 10, 2529. 10. Brzezinski, L. J.; Rafel, S.; Leahy, J. W. J. Am. Chem. Soc. , 1997, 119, 4317. 11. Dounay, A. B.; Urbanek, R. A.; Frydrychowski, V. A.; Forsyth, C. J. J. Org. Chem., 2001, 66, 925. 12.参考书:现代有机合成试剂<性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号