| 物竞编号 | 0LV3 |
|---|---|
| 分子式 | InBr3 |
| 分子量 | 354.53 |
| 标签 | 催化剂 |
编号系统
CAS号:13465-09-3
MDL号:MFCD00011057
EINECS号:236-692-8
RTECS号:暂无
BRN号:暂无
PubChem号:24878807
物性数据
1. 性状:白色的吸湿性晶状固体
2. 密度(g/mL,25/4℃):4.74
3. 相对蒸汽密度(g/mL,空气=1):未确定
4. 熔点(ºC):436
5. 沸点(ºC,常压):656
6. 沸点(ºC,5.2kPa):未确定
7. 折射率:未确定
8. 闪点(ºC):未确定
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC):不适用的
11. 蒸气压(kPa,25ºC):未确定
12. 饱和蒸气压(kPa,60ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:可溶解的
毒理学数据
生态学数据
通常对水体是稍微有害的,不要将未稀释或大量产品接触地下水,水道或污水系统,未经政府许可勿将材料排入周围环境。
分子结构数据
1、摩尔折射率:无可用的
2、摩尔体积(cm3/mol):无可用的
3、等张比容(90.2K):无可用的
4、表面张力(dyne/cm):无可用的
5、介电常数:无可用的
6、极化率(10-24cm3):无可用的
7、单一同位素质量:351.658868 Da
8、标称质量:352 Da
9、平均质量:354.53 Da
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:0
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积0
7.重原子数量:4
8.表面电荷:0
9.复杂度:8
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.常温常压下稳定
避免的物料 水分/潮湿
2.振动光谱指出每个铟原子以八面体方式被六个溴原子所包围。它在有机溶剂中的溶解度与氯化铟相似。
3.具有吸湿性。
贮存方法
阴凉干燥处隔绝空气密闭保存。
合成方法
1.用电解氧化法制取InBr3。在金属铟(0.5g)上的电压保持为+50V,溶液相为含有2g液态Br2、10mg[Et4N]Br的100mL苯甲醇混合物(体积比为3∶1)。苯在使用前要经过用钠-萘醌进行干燥和蒸馏(均在氮气氛下),甲醇是分析纯试剂。在整个实验过程中都要把电解池放在冰浴中进行冷冻,因为在反应中有可观的热量放出。
用干燥氮气吹洗电解池。电流为100mA,2.5h之后,停止通电。在反应器底部生成的棕色油液中不含铟并可以弃去。把上层清液小心地移入一只100mL圆底烧瓶中,并在室温下真空蒸发抽除溶剂,直到体积缩减到约15mL时为止。将得到的白色固体收集起来很快地用若干小体积的乙醚洗涤:虽然溴化铟(Ⅲ)能溶于乙醚,但是溶解速度相当慢,在此洗涤中的损耗是可以容许的。收集和洗涤晶体的操作都要在干燥的氮气氛下进行。产量为11g(79%)。依InBr3计算:In,32.4;Br,67.6。分析结果:In,32.1;Br,66.9。注意事项本合成使用了液态溴,所有的操作都应当在一座排风良好的通风橱中进行。对液态溴进行操作时应当极为小心。
2.通过在氮气和溴气氛下加热金属铟制备而来。
用途
InBr3是一个水溶性的绿色路易斯酸催化剂,能高化学选择性、区域选择性和立体选择性地用于多种类型的有机合成。相比于传统路易斯酸,InBr3对水汽稳定、可循环使用、操作简单、能够容忍含氧和含氮底物以及能够用于催化反应(如催化醛和缩醛的炔基化反应、Michael加成反应以及吲哚的磺化反应等),非常符合绿色化学的概念。
芳香胺与烯糖在InBr3催化下能够高产率和高立体选择性地生产苯并杂二环化合物 (式1)[1],为苯并杂环化合物的合成提供了一种简单高效的一步合成法。虽然该反应在InCl3作用下也能进行,但InBr3表现出了更强的催化活性。
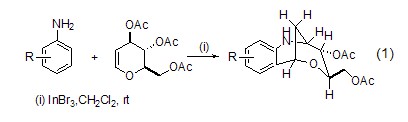
三乙基硅烷、烯酮和醛在InBr3催化下能够高产率地发生三组分羟醛缩合反应 (式2)[2],反应经历了原位产生氢化铟中间体以及其对烯酮的加成配位反应。
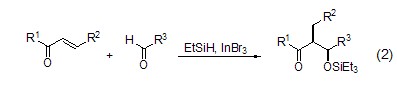
端炔底物与芳基碘化物在PdCl2(PPh3)2- InBr3催化体系作用下能够高产率地发生交叉偶联反应 (式3)[3],该方法能应用于2-苯基吲哚化合物的一步合成,即作用于2-苯基乙炔基苯底物,使其发生分子内环加成得到相应的吲哚产物。
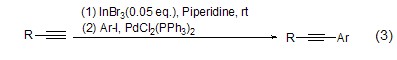
吲哚与醌在InBr3催化下能够发生共轭加成反应,得到3-吲哚醌化合物 (式4)[4],吲哚与萘醌也能在InBr3作用下发生类似反应。

α-取代的乙烯基芳烃在InBr3催化下能够有效发生二聚反应(式5)[5]。该反应的亮点在于能够通过调节取代基的类型来获得不同的二聚产物,如吸电子取代基的存在会导致开链二聚,而给电子取代基的存在则导致成环二聚反应。
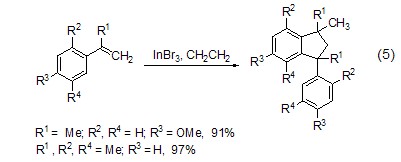
在催化量的InBr3存在下,苄基醇、烯丙基或苄基醋酸盐能与烯丙基硅烷发生脱氧烯丙基化反应,高产率地得到相应的烯丙基化产物 (式6)[6]。
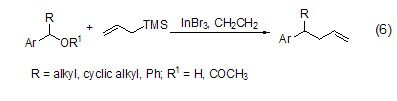
InBr3还能有效催化环氧化物与芳香胺的氨解反应,高产率地得到相应的β-氨基醇化合物 (式7)[7],这是合成天然产物的重要中间体。
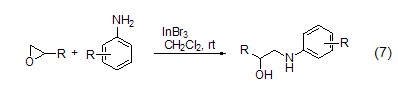
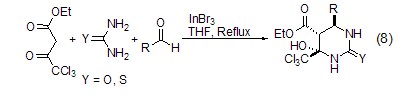
1,3-二羰基化合物与醛和尿素在InBr3催化下能发生Biginelli类型三组分成环缩合反应,高产率地得到带取代基的四氢嘧啶酮化合物 (式8)[8]。
安全信息
危险运输编码:暂无
危险品标志: 刺激
刺激
危险标识:R36/37/38
文献
1. Yadav, J. S.; Rao, K. V.; Raj, K. S.; Prasad, A. R.; Kunwar, S. K.; Kunwar, A. C.; Jayaprakash, P. J.; Jagannath, B. Angew. Chem., Int. Ed., 2003, 42, 5198. 2. Shibata, I.; Kato, H.; Ishida, T.; Yasuda, M.; Baba, A. Angew. Chem., Int. Ed., 2004, 43, 711. 3. Sakai, N.; Annaka, K.; Konakahara, T. Org. Lett., 2004, 6, 1527. 4. Yadav, J. S.; Reddy, B. V. S.; Swamy, T. Synthesis, 2004, 106. 5. Peppe, C.; Lang, E. S.; de Andrade, F. M.; de Castro, L. B. Synlett, 2004, 1723. 6. Kim, S. H.; Shin, C.; Pae, A. N.; Koh, H. Y.; Chang, M. H.; Chung, B. Y.; Cho, Y. S. Synthesis, 2004, 1581. 7. Rodriguez, R. J.; Navarro, A. Tetrahedron Lett., 2004, 45, 7495. 8. Martins, M. A. P.; Teixeira, M. V. M.; Cunico, W.; Scapin, E.; Mayer, R.; Pereira, C. M. P.; Zanatta, N.; Bonacorso, H. G.; Peppe, C.; Yuan, Y.-F. Tetrahedron Lett., 2004, 45, 8991. 9.参考书:现代有机合成试剂<性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号