| 物竞编号 | 0K13 |
|---|---|
| 分子式 | KNO3 |
| 分子量 | 101.10 |
| 标签 | 土硝, 火硝, 硝石, 盐硝, Nitric acid potassium salt, Saltpeter for technical, 高纯度化合物, 护色剂(发色剂) |
编号系统
CAS号:7757-79-1
MDL号:MFCD00011409
EINECS号:231-818-8
RTECS号:TT3700000
BRN号:暂无
PubChem号:24898742
物性数据
1.性状:无色透明斜方或三方晶系颗粒或白色粉末[1]
2.熔点(℃):334[2]
3.沸点(℃):400(分解)[3]
4.相对密度(水=1):2.11[4]
5.溶解性:易溶于水,溶于甘油,不溶于无水乙醇、乙醚。[5]
毒理学数据
1.急性毒性[6] LD50:3750mg/kg(大鼠经口)
2.刺激性 暂无资料
生态学数据
1.生态毒性 暂无资料
2.生物降解性 暂无资料
3.非生物降解性 暂无资料
4.其他有害作用[7] 该物质对环境有危害,应特别注意对水体的污染。
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:3
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积62.9
7.重原子数量:5
8.表面电荷:0
9.复杂度:18.8
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:2
性质与稳定性
1.约400 ℃时分解放出氧,并转变成亚硝酸钾,继续加热则生成氧化钾。在空气中不易潮解。为强氧化剂,与有机物接触能引起燃烧爆炸,并放出有刺激性气味的有毒气体。与碳粉或硫黄共热时,能发出强光和燃烧。
2.稳定性[8] 稳定
3.禁配物[9] 强还原剂、强酸、易燃或可燃物、活性金属粉末
4.避免接触的条件[10] 受热、潮湿空气
5.聚合危害[11] 不聚合
6.分解产物[12] 氮氧化物、氧气
贮存方法
储存注意事项[13] 储存于阴凉、干燥、通风良好的库房。远离火种、热源。库温不超过30℃,相对湿度不超过80%。应与还原剂、酸类、易(可)燃物、活性金属粉末分开存放,切忌混储。储区应备有合适的材料收容泄漏物。
合成方法
工业生产有复分解法和离子交换法。用氯化钾和硝酸铵(代替硝酸钠)为原料的复分解法,氯化钾和稀硝酸为原料的离子交换法和溶剂萃取法,氯化钾、硝酸铵、碳酸氢铵为原料的内循环法,硝酸铵、氯化钾为原料的循环法等工艺均处于工艺研究阶段。
1.复分解法 将硝酸钠加入盛有适量水的反应器中,用蒸汽加热,在搅拌下使硝酸钠全部溶解,再按NaNO3:KCl=100:85配料比缓慢加入氯化钾进行复分解反应,生成硝酸钾,当加热蒸发使溶液浓度达45~48°Bé、温度达120℃时,首先析出氯化钠。经真空过滤,用少量热水洗涤氯化钠晶体,减少硝酸钾的带损。滤液送入结晶器,用滤液量10%~15%的水稀释,边搅拌边冷却,经24h后,析出硝酸钾结晶,经真空过滤、水洗、离心分离后,送至气流干燥器在80℃以上进行干燥,制得硝酸钾成品。其反应方程式如下: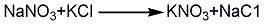
2.离子交换法 以氯化钾和硝酸铵为原料,使氯化钾和硝酸铵溶液中的钾铵离子在离子交换树脂上进行转换,得到硝酸钾溶液和氯化铵溶液。反应方程式如下:
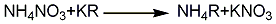
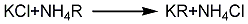
经蒸发浓缩、过滤、滤液冷却结晶,过滤,水洗、离心分离,气流干燥,制得硝酸钾成品。
3.工业上常利用氯化钾和硝酸钠的复分解反应制备,于500mL蒸发皿中加入100mL去离子水,加热到60℃,在搅拌下逐渐加入100g工业硝酸钾粉末。再加入0.1g碳酸钾,稍加煮沸,过滤,在搅拌下滤液冷却结晶,抽滤,干燥。
4.取100g硝酸钾溶于80mL热水中,溶液经折叠滤纸过滤,于搅拌下冷却,用布氏漏斗吸滤出结晶,并在室温下使之干燥,若母液加以利用,则制剂产率可达97%,溶液在过滤前若加入0.1gK2CO3(纯级),煮沸后过滤,可以除去杂质Fe3+,制剂中若含有杂质KNO2,可按下述方法处理。取400g硝酸钾溶于900mL水中,向此溶液中加入20mLHNO2,然后滴加入KMno4溶液,直到红色不退为止,再加1~3滴草酸溶液,使红色素退去,为了除去溶液中的Mn2+加入K2CO3至呈弱酸性,过滤析出MnCO3沉淀,滤液则用HNO3中和,直至呈中性。然后将溶液蒸发至形成结晶膜。以下结晶和分离等操作,可按上述方法进行。
5.转化法 系将硝酸钠与氯化钾复分解而得。此法工艺流程简单,产品质量较高,工业上广泛采用。
6.合成法 系按硝酸与氯化钾作用,生成硝酸钾、氯气及亚硝酰氯。
用途
1.分析试剂,用于锰、钠的微量分析。是制造黑色火药,如矿山火药、引火线、爆竹等的原料。也用于焰火以产生紫色火花。机械热处理作淬火的盐浴。陶瓷工业用于制造瓷釉彩药。用作玻璃澄清剂。用于制造汽车灯玻壳、光学玻璃显像管玻壳等。医药工业用于生产青霉素钾盐,利福平等药物。用于制卷烟纸。用作催化剂。选矿剂。用作农作物和花卉的复合肥料。
2.硝酸钾也是我国允许使用的发色剂。它在肉制品中由于细菌作用而还原成亚硝酸钾而起护色和抑菌的作用。我国规定可用于肉类制品,最大使用量0.5g/kg,残留量不得超过0.03g/kg。
3.广泛用于制造黑色火药、焰火,尤其是制造点火用的引火线、硝纸和爆竹。硝酸钾是很好的食品防腐剂,用于腌肉可长久保持新鲜,防止腐烂,还用于制造玻璃澄清剂、陶瓷釉彩药、催化剂的添加剂、金属淬火及盐浴等。
4.硝酸盐类均具有早强作用,尤其是在低温、负温时作为早强、防冻剂。是制造黑色火药的原料。机械热处理作淬火的盐浴。陶瓷工业用于制造瓷釉彩药。用作玻璃澄清剂。用于制造汽车灯玻壳、光学玻璃、显现管玻壳等。医药工业用于生产青霉素钾盐。还用作农作物和花卉的复合肥料。
5.在焦磷酸盐镀铜中添加硝酸盐可以提高工作电流的上限,能减少镀层针孔,降低溶液操作温度,提高均镀能力等,硝酸盐在光亮镀铜溶液中对整平作用和阴极效率略有降低。
6.用于制造烟火、火药、火柴、医药,以及玻璃工业。[14]
安全信息
危险运输编码:UN 1486 5.1/PG 3
危险品标志: 氧化剂
氧化剂  有害
有害  刺激
刺激
文献
[1~14]参考书:危险化学品安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8
备注
曾用CAS:7759-79-1



 沪公网安备 31010602001115号
沪公网安备 31010602001115号