| 物竞编号 | 0306 |
|---|---|
| 分子式 | C3H6O2 |
| 分子量 | 74.08 |
| 标签 | 蚁酸乙酯, 甲酸乙烷基, Formic acid ethyl ester, Formic ether, Ethyl methanoate, 杀菌剂, 杀幼虫剂, 熏蒸剂, 食品添加剂, 增香剂 |
编号系统
CAS号:109-94-4
MDL号:MFCD00003294
EINECS号:203-721-0
RTECS号:LQ8400000
BRN号:906769
PubChem号:24889112
物性数据
1.性状:无色易流动液体,有芳香气味。[1]
2.熔点(℃):-80[2]
3.沸点(℃):54.3[3]
4.相对密度(水=1):0.92[4]
5.相对蒸气密度(空气=1):2.55[5]
6.饱和蒸气压(kPa):25.6(20℃)[6]
7.燃烧热(kJ/mol):-1630[7]
8.临界温度(℃):235.3[8]
9.临界压力(MPa):4.74[9]
10.辛醇/水分配系数:0.23[10]
11.闪点(℃):-20(CC)[11]
12.引燃温度(℃):455[12]
13.爆炸上限(%):16.5[13]
14.爆炸下限(%):2.7[14]
15.溶解性:微溶于水,溶于苯、乙醇、乙醚等多数有机溶剂。[15]
16.黏度(mPa·s,15ºC):0.419
17.蒸发热(KJ/mol,54.15ºC):30.15
18.生成热(KJ/mol):369.28
19.比热容(KJ/(kg·K),15~30ºC,定压):2.00
20.沸点上升常数:2.086
21.电导率(S/m,20ºC):1.45×10-9
22.热导率(W/(m·K),12ºC):0.1583
23.体膨胀系数(K-1,20ºC):0.00141
24.临界密度(g·cm-3):0.323
25.临界体积(cm3·mol-1):229
26.临界压缩因子:0.257
27.偏心因子:0.285
28.Lennard-Jones参数(A):11.14
29.Lennard-Jones参数(K):161.3
30.溶度参数(J·cm-3)0.5:18.939
31.van der Waals面积(cm2·mol-1):6.440×109
32.van der Waals体积(cm3·mol-1):42.740
33.气相标准燃烧热(焓)(kJ·mol-1):-1639.7
34.气相标准声称热(焓)( kJ·mol-1) :-398.3
35.液相标准燃烧热(焓)(kJ·mol-1):-1607.5
36.液相标准声称热(焓)( kJ·mol-1):-430.5
37.液相标准热熔(J·mol-1·K-1):144.3
毒理学数据
1、刺激性:家兔经皮开放性刺激试验: 460mg,轻度刺激。
2、急性毒性:大鼠经口LD50:1850mg/kg;大鼠吸入LCLO:8000ppm/4H;兔子经口LD50:2075mg/kg;兔子皮肤LD50:>20ml/kg;兔子皮下LDLO:1gm/kg;豚鼠经口LD50:1110mg/kg;
3、致肿瘤:小鼠皮肤TDLO:110gm/kg/9W-I;
4、毒性较甲酸甲酯稍弱,猫吸入42420mg/m3的蒸气17分钟,会引起强烈的刺激,呼吸困难、眩晕,其后即能恢复;若达22分钟时,则因肺水肿而致死。999.9mg/m3能强烈地刺激人的鼻和轻度刺激眼睛。工作场所最高容许浓度300mg/m3空气。
5.急性毒性[16]
LD50:1850mg/kg(大鼠经口);20000mg/kg(兔经皮)
6.刺激性[17]
家兔经皮:460mg,轻度刺激(开放性刺激试验)
生态学数据
1.生态毒性 暂无资料
2.生物降解性 暂无资料
3.非生物降解性[18] 空气中,当羟基自由基浓度为5.00×105个/cm3时,降解半衰期为11d(理论)。
当pH值为7,8时,水解半衰期分别为3.1d,7.5h(理论)。
4.其他有害作用[19] 该物质对环境可能有危害,对水体应给予特别注意。
分子结构数据
1、摩尔折射率:17.87
2、摩尔体积(cm3/mol):81.7
3、等张比容(90.2K):180.0
4、表面张力(dyne/cm):23.5
5、极化率(10-24cm3):7.08
计算化学数据
1.疏水参数计算参考值(XlogP):0.5
2.氢键供体数量:0
3.氢键受体数量:2
4.可旋转化学键数量:2
5.互变异构体数量:无
6.拓扑分子极性表面积26.3
7.重原子数量:5
8.表面电荷:0
9.复杂度:26.1
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.化学性质:甲酸乙酯易水解,空气中的湿气作用下也能水解成甲酸和乙醇而呈酸性。在酸、碱存在下能促进水解。加热至300℃以上分解生成乙烯、甲酸、一氧化碳、二氧化碳、氢、水和甲醛。在氯化铁存在下加热至150℃分解得到乙醚、一氧化碳。在镍存在下加热至150~300℃生成一氧化碳、氢、甲烷及不饱和烃。氧化铝也能促进甲酸乙酯的热解。与五氧化二磷反应得到二氯甲基乙基醚。在三氯化铝存在下与苯反应生成乙苯、1,3-二乙基苯、1,3,5-三乙基苯。在三氟化硼存在下与苯反应主要生成乙苯。在氢氧化钾存在下与丙酮在醚溶液中反应生成α羟基异丁酸。甲酸乙酯在醚溶液中也能与Grignard试剂反应,生成各种相应的化合物。例如与叔丁基氯化镁在-10~-15℃反应,生成三甲基乙醇,副产物为三甲基乙醛。甲酸乙酯能与Lewis酸、四氯化锡、四氯化钛、五氯化锑、三氯化铝等生成复合物。
2.稳定性[20] 稳定
3.禁配物[21] 强氧化剂、碱
4.聚合危害[22] 不聚合
贮存方法
储存注意事项[23] 储存于阴凉、干燥、通风良好的库房。远离火种、热源。库温不宜超过29℃。保持容器密封。应与氧化剂、碱类分开存放,切忌混储。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工具。储区应备有泄漏应急处理设备和合适的收容材料。
合成方法
1.硫酸酯化法甲酸与乙醇在硫酸催化下直接酯化,经中和水洗后精馏得成品。
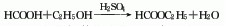
2.三氯化铝催化酯化法由甲酸和乙醇在结晶三氯化铝催化剂存在下酯化而得。
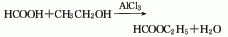
3.由乙醇和甲酸在硫酸存在下加热酯化后,用五氧化二磷或无水氯化钙脱水精馏而得。
精制方法:由于甲酸乙酯易水解,因此常含有游离的甲酸和乙醇并显酸性。精制时先用碳酸钠溶液洗涤,再用无水碳酸钾或五氧化二磷干燥、分馏。氯化钙与甲酸乙酯形成结晶性复合物,不宜用作干燥剂。
4.制法:
于装有回流冷凝器的反应瓶中,加入98%的甲酸61g(1.33mol),无水乙醇(2)31g(0.67mol),一粒沸石,加热回流反应24h。改为蒸馏装置进行蒸馏,收集62℃以下的馏分,溜出液用氯化钠饱和,再依次用饱和碳酸氢钠、饱和氯化钠溶液洗涤。无水硫酸钠干燥,分馏,收集53~54℃的馏分,得甲酸丁酯(1)36g,收率72%。[25]
用途
1.甲酸乙酯用作硝酸纤维素、乙酸纤维素等的溶剂,以及食品、香烟、谷类、干燥果品等的杀菌剂、杀幼虫剂和熏蒸剂。甲酸乙酯作为香精可用于调合桃子、香蕉、苹果、杏、菠萝、浆果等香气,亦可作为黄油、白兰地酒、甜酒、威士忌酒等的香料。甲酸乙酯也是有机合成的中间体。例如在制药工业,用于抗肿瘤药物富雪定、维生素B1的生产;甲酸乙酯与丙酮在甲醇钠-二甲苯溶液中缩合可得乙酰基乙烯醇钠,与乙酰甘氨酸酯缩合再与硫氰化钾环合可得2-巯基咪唑-4-羧酸乙酯。甲酸乙酯用于生产鱼腥草素、痛惊宁、康复龙、噻嘧啶、噻啶苯芥、利血生、全合成法山莨菪等的药物。
2.用作醋酸纤维素和硝酸纤维素的溶剂,以及用于香精合成和医药生产。[24]
安全信息
危险运输编码:UN 1190 3/PG 2
危险品标志:暂无
文献
[1~24]参考书:危险化学品安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8 [25]参考文献:Furniss B S,Hannaford A J,Rogers V,et al. Vogel’s Texbook of Practical Chemistry. Longman London and New YorK. Fourth edition,1978:507. 参考书:有机化合物合成手册/孙昌俊,王秀菊,孙风云主编. 北京:化学工业出版社,2011.8 ISBN 978-122-11519-5
备注
暂无








 沪公网安备 31010602001115号
沪公网安备 31010602001115号